ابتكار مستقبلات تجميعية ومرنة قادرة على الارتباط بأي مستضد
02 February 2025
نشرت بتاريخ 2 فبراير 2025
يوفر النظام PAGERs مستقبلات للاقتران بالبروتين G تتميز بتصميمها التجميعي المرن لأغراض الدراسات المتعلقة بمسار الإشارات الخلوية.
Credit:JUAN GAERTNER / SPL/ GETTY IMAGES
تحظى مستقبلات سطح الخلية بأهمية بالغة في استشعار الخلايا للبيئة المحيطة بها واستجابتها لها. وعند ارتباط هذه البروتينات الممتدة عبر الأغشية بجزيئات كيميائية خارج الخلية، فإنها تحفز التتابُعات الإشارية أو تؤدي إلى نَسخ جين جديد، وهو ما يفضي في النهاية إلى تغيرات في سلوك الخلية نفسها.
وتُعد المستقبلات المقترنة بالبروتين G (التي تُعرف اختصارًا بمستقبلات GPCRs) أكبر عائلات المستقبلات البشرية وأكثرها تنوعًا، ويرمّزها 800 جين مميز على أقل تقدير. وبالنظر إلى الدور الذي تؤديه معظم هذه المستقبلات في القدرة على التذوق وتمييز الروائح ورؤية الضوء، فإن التحكم بها قد يتيح للباحثين أيضًا التحكم بشكل فعال في نشاط خلاياها. غير أن ذلك يتطلب عملًا شاقًا ومضنيًا يتضمن إدخال طفرة تلو الأخرى على مُستقبل واحد فحسب في كل مرة، وإخضاعه لعملية تطور موجَّه؛ وهو ما يعني عدم الاستفادة من إمكانات مستقبلات GPCRs المُخلَّقة.
وقد تمكن باحثون من جامعة ستانفورد بكاليفورنيا وجامعة بكين بالعاصمة الصينية بكين من تطوير نظام تجميعي مرن وقابل للتعديل يهدف إلى تخليق مستقبلات بسهولة يمكنها الاستجابة إلى أي رُبيطة تحظى باهتمام الباحثين وإنشاء استجابة من بين العديد من الاستجابات الناتجة المحتملة. وقد أفردت دورية Nature، في مقالة نشرتها في وقت سابق من هذا الشهر (انظر: التواصل مع باطن الخلايا)، وصفًا دقيقًا لتلك الأداة التي تُسمى مستقبلات المستضدات المقترنة بالبروتين G المبرمجة والمعدلة وراثيًا (والمعروفة اختصارًا باسم PAGERs).
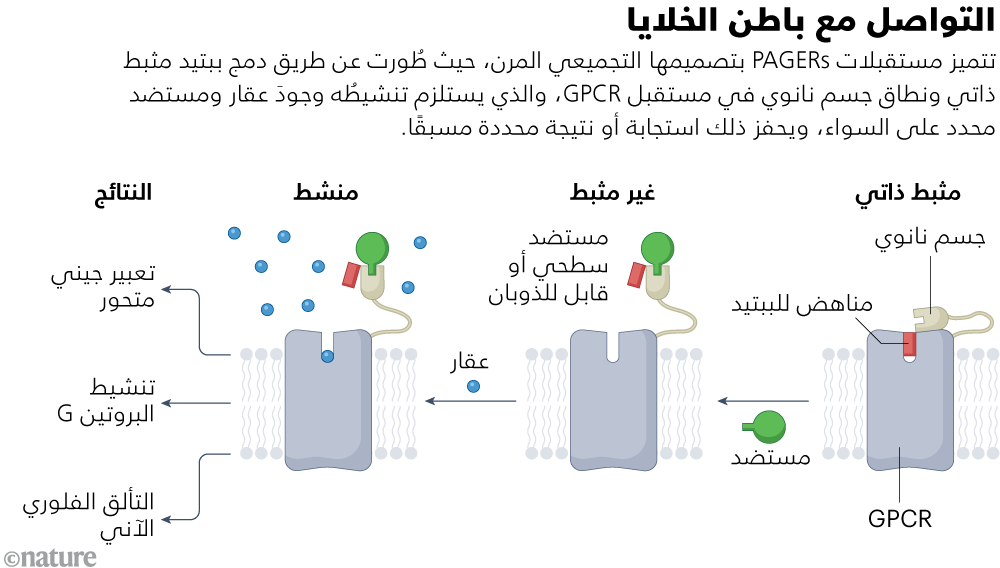
إضافة قوية للمستقبلات المخلَّقة
استفاد الفريق البحثي في تطوير مستقبلات PAGERs من تقنية قائمة بالفعل تُسمى المستقبلات المصممة خصصيًا لتنشيطها باستخدام عقاقير معينة (المعروفة اختصارًا باسم DREADDs)؛ وهي مستقبلات طورها براين روث، عالم البيولوجيا التخليقية في جامعة نورث كارولينا بتشابل هيل، في مختبره عام 2007؛ وهي عبارة عن مستقبلات GPCRs مُخلَّقة لا تَنْشَط إلا داخل الخلايا أو في أجساد الحيوانات المعدلة وراثيًا حال إعطائها عقار محدد. ويُعتمَد على هذه المستقبلات على نطاق واسع في مجال علم الأعصاب من أجل "تحليل دوائر الدماغ المسؤولة عن السلوك والوظائف الأخرى"، على حد وصف روث.
ما يميز دراسة مستقبلات PAGERs، من وجهة نظر روث، يكمن في كونها المرة الأولى التي يرى فيها فريقًا بحثيًا يستعين بمستقبلاته من أجل ابتكار تقنية جديدة. يقول: "عندما وصلتني هذه الورقة البحثية وبدأت في قراءتها، قلت لنفسي: يا إلهي! كيف لم تخطر مثل هذه الفكرة ببالي من قبل؟ إنها حقًا مذهلة!"
ولتخليق مستقبلات PAGERs، عمد الفريق البحثي، بقيادة آليس تينج، عالمة البيولوجيا الكيميائية، إلى دمج مكونين اثنين بالجزء خارج الخلوي للبنية الأساسية لمستقبل DREADD؛ وهما نطاق مثبط ذاتي وجسم نانوي (شذرة دقيقة من جسم مضاد) يمكنه الارتباط بالمستضد محل اهتمام الباحثين.
أما الجزئ الناتج، فيكون نشاطه "مرهونًا بوجود المستضد"؛ وفي حالة غياب ذلك المستضد، الذي ربما يكون جزيئًا قابلًا للذوبان أو مثبتًا على سطح خلايا آخرى، فإن نطاق المثبط الذاتي يكبح نشاط التجويف المسؤول عن الارتباط بالمُستقبِل، ويحول دون تنشيطه حتى في حال وجود العقار. وعند ارتباط المستضد بالجسم النانوي، ينفصل النطاق المثبط الذاتي عن المُستقبِل مفسحًا المجال لتنشيطه بواسطة العقار. وهذا التحكم الصارم متعدد المستويات يتيح للباحثين ضبط الخصائص الزمانية والمكانية للاستجابات داخل الخلايا التي تعبر عن بروتينات مستقبلات PAGER.
وأشار جوش ليونارد، اختصاصي البيولوجيا التخليقية بجامعة نورث ويسترن في مدينة إيفانستون بولاية إلينوي الأمريكية، إلى فائدة سريرية، من جملة فوائد أخرى، يمكن تحقيقها بفضل هذه الأداة عن طريق تمكين الباحثين من زيادة فعالية بعض العلاجات أو الحد من نشاطها وفعاليتها في حالة حدوث رد فعل سلبي، قائلًا: "لا شك أن القدرة على تنشيط فعالية علاج خلوي من هذا القبيل أو تثبيطها باستخدام الأدوية والعقاقير تتيح لنا ميزة مثالية".
ويمكن القول إن النهج التجميعي المرن لنظام مستقبلات PAGERs يُعزى في الجانب الأكبر منه إلى الجسم النانوي الملحق بتلك المستقبلات؛ وذلك لأن التشابه بين الأجسام النانوية التي ترتبط بالمستضدات المختلفة من حيث الحجم وخصائصها الهندسية يتيح للباحثين استبدال ذلك الجسم النانوي بسهولة ليحل محله جسم نانوي آخر بغية استهداف أي مستضد يكون له جسم نانوي ملائم. وقد صمم فريق تينج البحثي مجموعة من النماذج المتفاوتة لتلك المستقبلات التي اشتملت على جزيئات قادرة على الاستجابة لبروتينات فلورية وعوامل نمو وبروتينات سطح الخلية.
كما استطاع الباحثون التحكم في النتائج المترتبة على تنشيط مستقبلات PAGERs عن طريق اختيار بنية أساسية لتلك المستقبلات ذات وظيفة مستفعلة ملائمة للغرض. وقد أثبت الفريق البحثي فعالية تصميمات تلك المستقبلات وقدرتها على تنشيط جين متحور، أو بدء التتابعات الإشارية، أو تحفيز الوميض الفلوري واستخدامه كمستشعر.
تقول تينج: "ما نسعى إليه هو أن يكون لدينا منظومة من المستقبلات المُخلَّقة القادرة على الاستجابة إلى أي مستضد خارج خلوي قد نختاره، ثم تحفيز العديد من الاستجابات خارج الخلوية التي يختارها الباحث باستخدام هذه البنية الأساسية لمستقبلات GPCRs".
في واحدة من التجارب، مثلًا، وجد الباحثون أن استخدام مستضد ورمي محدَّد يحفز إفراز بروتين يساهم في قتل الخلايا السرطانية؛ فيما أدى استخدام مستقبلات PAGERs أخرى إلى هجرة الخلايا المناعية إلى مستضد محل لاهتمام للباحثين، أو تنشيط الخلايا العصبية التي تستشعر المستضدات.
يقول ليونارد: "تقنية المستقبلات المُخلَّقة التي نحن بصددها مثيرة للإعجاب حقًا، وأعتقد أنها تنبئ عن اتجاه مثير في هذا المجال". وتابع قائلًا إنه مع تطور البيولوجيا التخليقية واتجاهها لتصبح "تخصصًا هندسيًا أكثر رسوخًا ووضوحًا"، يتجه الباحثون إلى مرحلة تتجاوز البحث والاستكشاف، وتتعدَّاهما إلى تطوير تقنيات قوية ونافعة على نطاق واسع.
وقد قدم فريق تينج المواد والمكونات المتعلقة بمستقبلات PAGERs إلى مؤسسة »آدجين« Addgene، لإدراجها ضمن قاعدة بياناتها المتعلقة بالبلازميدات.
doi:10.1038/nmiddleeast.2025.11
تواصل معنا: