
微生物叢と宿主の相互作用の将来のイノベーションに向けて
幼少期の微生物叢を調べるプロジェクトによって、人生のこの重要な時期における微生物叢の影響についての新たな知見が得られるだろう。
微生物叢と宿主の相互作用の将来のイノベーションに向けて
人生の重要な時期である幼少期の間のマイクロバイオームについて、3件のプロジェクトがさまざまな角度から調べる。
原文:Towards future innovation in microbiota–host interactions
Global Grants for Gut Health(GGGH)プログラムは今年も、宿主と微生物叢の相互作用の新規メカニズムの解明を通じてヒトの健康を増進するための新たな手法の開発に寄与する研究プロジェクトを支援する。2021年は、「ヒトの健康における乳幼児期の微生物叢」をテーマとする3つの新規プロジェクトが採択となった。小児期に確立された微生物叢は、成人期の微生物叢の構成に影響することが知られている。つまり、小児期に確立された微生物叢がさまざまな疾患の感受性に大きく影響するのである。しかしながら、小児期の微生物叢が成人の健康にどのように影響するかはよくわかっていない。喜ばしいことに、今年も乳幼児期の微生物叢の解析に焦点を合わせた多くの応募があった。新型コロナウイルス感染症(COVID-19)のパンデミックが続く中、GGGHの審査委員会はオンラインで徹底的な議論を行い、その結果、優れた3件の提案を選出した。
デューク大学(米国)のローレンス・デビッド(Lawrence David)が提案した研究プロジェクトは、「乳児の微生物叢の代謝の食事性の決定因子」である。成人の腸内細菌叢に比べると、乳児の腸内細菌叢は生後2年間で大きく変化する。しかし、乳児期の腸内細菌叢がどのような機構で変化するのかは不明である。彼は、食事(特に食事性植物)が、微生物叢の組成や代謝に与える影響を解明することを目標にしている。この研究では、DNAシーケンシングに基づいた食物摂取量の検出法や、培養に基づくハイスループットなアッセイといった独自の分析手法を用いる。
ワーゲニンゲン大学(オランダ)のジェラード・ブライアン・ゴンザレス(Gerard Bryan Gonzales)が提案した研究プロジェクトは、「腸内微生物叢がほぼ一生の間の成長に及ぼす影響への経路のマッピング:成長変動リスクの高い集団における長期研究(Path2Growth)」である。生後の最初の2年間に栄養失調を経験すると、成人になってから疾患を発症するリスクが高いと考えられている。彼の研究は、微生物叢由来の代謝物であるホスファチジルコリンや多価不飽和脂肪酸と成長の間の相関に基づいて、ケニアとマラウイで100人以上の子どもを対象にこれらの代謝物と腸内細菌叢を分析し、腸内の代謝と乳児の成長の関連を明らかにすることを目指している。
ミシガン州立大学(米国)のロバート・クイン(Robert Quinn)が提案した研究プロジェクトは、「成長中のヒト腸における微生物産生抱合胆汁酸の役割の解明」である。一次胆汁酸は、肝臓でグリシンやタウリンと抱合することがよく知られている。しかし最近、抱合胆汁酸は、腸内細菌叢でも産生されていて、乳児に多く存在することが明らかになった。微生物が産生するこうした抱合胆汁酸は新規細菌代謝物であり、その生理作用はわかっていなかった。彼の研究は、微生物叢によって産生されるこうした抱合胆汁酸が健康に影響を与えるメカニズムを明らかにしようとするものだ。
これら3つの研究プロジェクトは極めて素晴らしいものであり、乳幼児期に腸内細菌叢が形成されるメカニズムや、そうした機構が成人の腸内細菌叢のどのような影響を与えるかを理解するのに大いに貢献すると確信している。こうした理解が進むことによって、最終的にヒトの健康増進につながるだろう。最後に、提案の評価に時間と労力を割いていただいた審査委員のティナ・ラスク・リヒト(Tine Rask Licht)、エラン・エリナフ(Eran Elinav)、ポール・W・オトゥール(Paul W. O’Toole)、カレン・P・スコット(Karen P. Scott)、趙 立平(Liping Zhao)に、心よりお礼を申しあげる。
腸内微生物叢が産生する胆汁酸を探る
2020年、ロバート・クイン、ピーター・ドレスタインらは、腸内微生物叢と胆汁酸の化学的理解に関して重要なブレークスルーを果たした。腸内微生物がさまざまなアミノ酸を胆汁酸に抱合させて、これまで全く知られていなかった多様な分子群を生成していることを明らかにしたのだ。クインは、GGGHの支援を得て、微生物性抱合胆汁酸(MCBA)がどのように生じ、それが人体にどのような影響を与えているのかについて、さらに詳しく調べる予定だ。
原文:Exploring bile acids produced by gut microbes

ロバート・クイン(Robert Quinn)
ロバート・クインは、アメリカンロブスターの細菌性甲殻病を研究したルイジアナ大学ラフィエット校(米国)で博士号を取得。サンディエゴ州立大学(米国)では、博士研究員として嚢胞性線維症の肺疾患に傾注。次いで、カリフォルニア大学サンディエゴ校(米国)で先進的なメタボロミクス法を研究。現在教職に就いているミシガン州立大学では、微生物生態学の理論とメタボロミクスを利用して、嚢胞性線維症の肺、ヒトの腸、およびサンゴ礁における微生物叢の動態を調べている。
MCBAをどのように発見したのか?
クイン: 胆汁酸が初めて化学的に記述されたのは1849年で、1927年にはハインリッヒ・ヴィーラント(Heinrich Wieland)が、その化学的性質を包括的に記述したことでノーベル化学賞を受賞しました。その記述には、胆汁酸合成の最終段階である、肝臓によるタウリンやグリシンというアミノ酸の抱合が含まれていました。ほぼ1世紀を経て、私たちの発見により、胆汁酸のアミノ酸抱合はこれまで考えられていたよりもはるかに複雑な過程であって、その多くは体内の微生物叢によって行われていることが明らかになりました。私たちは、動物の全身の生化学に対する微生物叢の全体的な影響を調べていて、こうした分子を発見しました。私たちは、ドレスタイン研究室で開発された先進的なメタボロミクス技術を用いて、無菌マウスと通常のマウスの代謝物を比較しました。無菌マウスと通常マウスの29種類の器官を調べて両群の比較を行うことで、微生物叢に特有の分子を見つけようとしたのです。この膨大なデータセットを1年かけて探索した結果、微生物叢を持つマウスに特有の未知の胆汁酸が3種類見つかりました。質量分析データの分析から、これらの胆汁酸のコアに、独特なアミノ酸が結合していることがわかりました。私たちはすぐさま、ほとんどの抱合胆汁酸とは異なり、こうしたMCBAは肝臓ではなく腸内微生物に由来のものであることに気づきました。
このプロジェクトで調べるものとは?
クイン: 生体の働きは意味もなく進められているわけではありません。MCBAを産生するに当たって腸内微生物叢には何らかの選択圧がかかっていると考えられます。その理由が問題です。今回のプロジェクトでは、MCBAがどのように作られ、それがヒト腸にどのような影響を与えているのかを明らかにしたいと考えています。このプロジェクトには3つの局面があります。(1)Enterocloster bolteaeという腸内細菌はさまざまな胆汁酸を抱合する能力を持つことがわかっているため、原因酵素を見つけるためにそのゲノムを探ります。(2)MCBAがなぜ、ヒトをはじめとする哺乳類の糞便中に広く見られるのか、とりわけその一生の早い時期に見られるのかを明らかにし、それらが健康に対して果たす役割を調べたいと考えています。私たちは、発育期の乳幼児から収集した1400点の糞便試料を対象としてミシガン大学の共同研究者ジュリー・ルメング(Julie Lumeng)がメタボローム解析を行うことで、MCBAを発見しました。糞便中にMCBAが存在することと、この乳幼児集団の発育および健康状態との関連を明らかにしたいと思います。この研究で中心となるのは、私のもとで研究する大学院生のダグラス・グジオール(Douglas Guzior)です。(3)ミシガン州立大学で樹立した新しいノックアウトマウスモデルを使って、発育中のマウス腸に対するMCBAの影響をさらに調べる計画です。
このノックアウトマウスモデルの特徴は?
クイン: 先述したタウリン・グリシン抱合胆汁酸は、胆汁酸補酵素A:アミノ酸N-アシルトランスフェラーゼ(BAAT)という肝臓の酵素の働きによって作られます。ヒトやマウスの腸にはBAATの働きで作られたタウリン・グリシン抱合胆汁酸が大量にあり、私たちの微生物性胆汁酸を調べる上ではこれが邪魔になります。微生物性胆汁酸の存在量はその10分の1~50分の1程度なのです。このため私たちは、そうしたタウリン・グリシン抱合胆汁酸を持たないBAATノックアウトマウスを作製しました。このBAATノックアウトマウスの腸にMCBAを導入することで、もっと明確にMCBAの生物学的性質を調べることができると思います。極めて大量の肝臓由来の抱合胆汁酸を排除することで、MCBAに特有と考えられる消化器系の健康と疾患の側面を調べることが可能になります。このBAATノックアウトモデルは、このプロジェクト以外でもいくつかの応用法があります。例えば、コレラやClostridioides difficileなどの多くの腸内感染症の病原体は、特定の胆汁酸の存在下でのみ出現するため、BAATノックアウトマウスは、こうした感染症を研究する上で有用なモデルとなるでしょう。
MCBAの腸への影響は良い? 悪い?
クイン: 両方の可能性があり、抱合されるアミノ酸次第でしょう。細菌によって、多様なアミノ酸はすべて胆汁酸へ抱合され、その結果生じるMCBAの化学的性質は極めて多様です。例えば、細菌がフェニルアラニンのように大きな疎水性アミノ酸を利用すると、その分子が強力な抗菌物質になるというエビデンスがあります。その細菌が、例えばセリンのようなもっと小さな親水性アミノ酸の抱合を行えば、その抗菌活性は失われます。クローン病の患者にはMCBAが多いことがわかっていますが、それが原因なのか結果なのかはまだわかっていません。MCBAは高脂肪食を摂取したマウスにも多いのですが、その理由もやはり不明です。MCBAは人間にとって益でもあり害でもあります。抱合の化学はとても重要なものと考えられます。
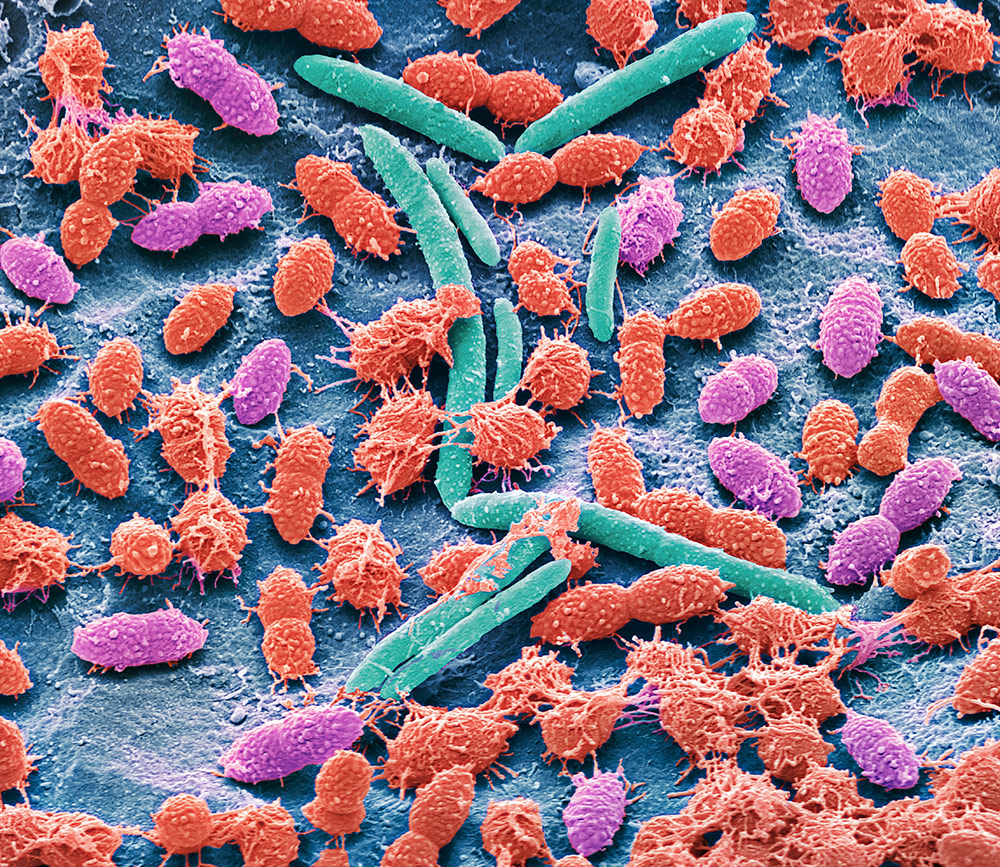
Steve Gschmeissner Science Photo Library/Science Photo Library/Getty
MCBAにはどのように有用か?
クイン: 私たちは、MCBAや、MCBAを作る細菌は、有望な薬物候補になると思います。いわゆる「薬としての微生物(bugs as drugs)」です。有用な特性を持つ特定のMCBAを産生するために、細菌の活動を操作できるかもしれません。例えば、ある種の胆汁酸は体に悪いことがわかっているため、それが糞便中に排泄されると有益でしょう。MCBAは糞便中に容易に排泄されるというエビデンスがありますので、有害な胆汁酸の抱合を行わせてその排泄を促進するよう細菌を改変できれば、多くの疾患の治療法となる可能性があります。
今後の計画は?
クイン: 短期的には、胆汁酸のシグナル伝達と代謝に関する理解を深めて、MCBAが宿主とどう相互作用し、どんな影響を与えるのかを明らかにしたいと考えています。より長期的で幅広い目標は、この知識を利用して新しいプロバイオティクスを開発することです。MCBAを産生する細菌を利用して特定の有益な特性を持つ分子を作らせることができれば、新たな治療選択肢となるでしょう。
最後になりますが、私は自分が腸内微生物叢を研究することになろうとは思ってもいませんでした! 以前は、肺疾患を主に研究していたのです。他の若い科学者へのメッセージとして、自分の研究の中で何か特別なものを発見したら、それが専門外の領域だと感じても、追求してほしいと思います。それは、科学においてワクワクする最高の瞬間なのです。
栄養不良が小児の成長をどう阻害するのかを微生物叢から明らかにする
腸内微生物叢は2つの重要な食物栄養素の利用可能性にどのような影響を与えているのだろうか。そして、栄養不良児の成長パターンにはどのような影響があるのだろうか。こうした疑問を抱いたブライアン・ゴンザレスは、GGGHの支援を得て、マラウイのマーティン・ムワンギらと共にその解明に取り組む。
原文:Discovering how malnutrition stunts children’s growth via the microbiome

ジェラード・ブライアン・ゴンザレス(Gerard Bryan Gonzales)
ジェラード・ブライアン・ゴンザレスは、フィリピン大学ミンダナオ校で食品工学を研究。食品科学修士号を得たのち、応用生物科学の博士号を取得するべく、ゲント大学(ベルギー)で質量分析法を用いてポリフェノールを研究。トルクメニスタンでWHO欧州の短期コンサルティング職を経験した後、ゲント大学でフランダース研究財団(Research Foundation Flanders)のフェローシップを得て、小児期の重度栄養不良のさまざまな表現型をつかさどる分子機構を研究。2020年、栄養情報科学・代謝学の助教としてワーゲニンゲン大学(オランダ)に着任。
GGGHプロジェクトの目的は?
ゴンザレス: アフリカのサハラ以南地域と南アジアでは、成長遅滞が極めて大きな負担になっています。成長遅滞とは、小児の体重と身長が世界保健機関(WHO)の定める基準に達していない状態です。成長阻害は慢性的な栄養不良によって生じます。そして、生後数カ月から数年間の栄養不良は、成人になってから非伝染性疾患が発症するリスクを高めます。栄養不良の影響を解消するのは極めて困難ですが、予防するためにできることはたくさんあります。最近の研究で私たちは、栄養の摂取と関連する成長の決定因子を特定する目的で、出生から2歳になるまで小児のコホートを追跡しました。その結果、コリンと多価不飽和脂肪酸(PUFA)という2つの必須食物栄養素が、小児の成長パターンと強力かつ一貫した関連をもっていることがわかりました。今回のGGGHプロジェクトでは、低中所得国の小児にコリンとPUFAのサプリメントを提供する複合的な栄養補給戦略を支持するエビデンスをさらに発見したいと考えています。
コリンとPUFA、それらと腸内微生物叢の発達との関連についてこれまでにわかっていることは?
ゴンザレス: コリンとPUFAはどちらも腸内微生物叢にとって重要な基質であり、腸内微生物叢によって代謝され、人体にとって極めて重要な別の化合物を生じます。コリンは微生物叢によって代謝されてトリメチルアミンとなり、それが肝臓で酸化されるとトリメチルアミン-N-オキシドが生じます。どちらかの代謝物濃度が上がりすぎると全身の炎症が引き起こされ、肥満をはじめとするメタボリックシンドロームにつながります。一方で、肉類などの高コリン食の摂取不足は成長遅滞を来します。私たちは、経時的にみると、腸内微生物叢が小児においてコリンとPUFAの代謝物の代謝(ひいては利用可能性)を規定していて、成長パターンに影響を与えているのだろうと考えています。
このプロジェクトでもたらされる新知見は?
ゴンザレス: これまでの栄養科学研究は、欧米の問題に着目したものがほとんどでした。世界では肥満児よりも低栄養児のほうが圧倒的に多いにもかかわらず、栄養不良の健康面の負担を取り扱う論文は相対的に少数だったのです。低中所得国の小児について考える研究はこれまで極めて少なかったので、今回の機会を得て私たちの研究を発展させ、より詳細なデータを収集できることをうれしく思っています。
どうやって答えを導くのか?
ゴンザレス: コリンとPUFAの代謝物は、血漿や糞便の試料に含まれています。私たちは、マラウイの生後2歳までの小児の既存のコホートから、その2つの栄養素に関して長期的なデータを収集する予定です。個々の参加者の極めて動的な消化器系からスナップショットをとることとなりますが、この長期的な側面が極めて重要です。私たちは、個々の小児について複数の試料を分析することで、小児の腸内微生物叢が時間とともにどう成熟するのか、そしてそれがコリンの代謝や成長にどのように影響するのかを見ていきます。また、ケニアでの既存の臨床試験で得られた試料の分析も行います。この臨床試験では、栄養不良から回復する小児を対象に抗生物質またはプラセボが6カ月にわたって毎日投与されました。この研究は、栄養不良と関連する特定の臨床状況における腸内微生物叢の役割を調べられるまたとない機会となります。重度の栄養不良で入院している小児には、生存の可能性を高める目的で抗生物質を投与するのが標準的な処置です。私たちは、このコホートの腸内微生物叢の成熟度を調べることに興味があります。
このプロジェクトでは予想される課題は?
ゴンザレス: 大きな課題はロジスティクスです。マラウイの現場は遠隔地であるため、コールドチェーンの維持や、試料の正確な収集、保存、輸送の確保が容易ではありません。マラウイの協力者が質の高い試料採取を終始徹底してくれるのはすばらしいことです。また、重要なのは、私たちが一般的にいうところの貧困の中で活動していることを忘れないようにしておくことです。こうした小児の栄養不良は原因がさまざまであり、環境もその小さな体に影響を与えています。環境汚染、感染症、極端な気象事象などがその例です。小児は、腸内微生物叢や成長・発達に影響しかねないさまざまな内的、外的要因にさらされています。また、糞便試料の収集にも制限があります。現地の文化でまだタブーとされている行為であるため、試料の定期的な提供を約束してもらうのが難しいのです。私たちの目的を説明してくれる地元のソーシャルワーカーの支援を得て、プロジェクト期間中に小児1人当たり5~6点の試料を収集したいと考えています。

Jeffrey Davis/Tetra images/Getty
この研究の実際的な応用法は?
ゴンザレス: 理想的には、支援してくれたコミュニティーに成果を還元できればと思っています。腸の健康を増進する安価で手に入りやすいサプリメントを小児に提供するなど、実行可能な介入法に発展させたいと考えています。この研究で得られたエビデンスを裏付けとしてさらに大規模な臨床試験を実施し、的確な介入法を見いだしたいと思います。さらに重要なこととして、マラウイの現地の科学者をトレーニングし、自分のコミュニティーで研究を行うための知識とツールを身につけてもらいます。自国の何が問題なのかがわかっている人たちですから、腸内微生物叢研究やメタボロミクス技術を応用して、そうした問題を解決してくれることでしょう。地元の問題を自分たちで直接解決する手段を科学者に提供することが、私の強い願いです。
将来の計画は?
ゴンザレス: 抗生物質の投与が行われているかどうかによらず、栄養不良児の微生物叢は根本的に変わってしまっていると考えられます。腸内微生物叢がコリンとPUFAの代謝物の利用可能性を制御することによって成長に影響を与えていることが実証されれば、食用サプリメントだけでなく、小児の腸の総合的な健康状態について考えることも必要になります。栄養不良児の腸内微生物叢のバランスをさらに細かく調べることになるかもしれません。究極的には、この小児のコホートをさらに長く、できれば青年期まで追跡するための資金が得られればうれしく思います。そうなれば、幼少期の微生物叢が性と生殖に関する健康や特定の疾患の発症に、どのような影響を与えるのかを知るのに役立つでしょう。
幼児の腸の発達に植物の力を利用する
ローレンス・デビッド、シルビア・ベッカー=ドレプス、テレサ・マクドナルドらは、ニカラグアのフィレモン・ブカルドおよびサムエル・ヴィルチェスと共に、GGGHの支援を得て、ニカラグアの幼児が摂取している植物性食物の多様性を評価し、それが腸内微生物叢の成熟と小児の総合的な健康状態にどう影響するのかを明らかにしようとしている。
原文:Tapping into the power of plants for the developing infant gut

ローレンス・デビッド(Lawrence David)
ローレンス・デビッドは、コロンビア大学(米国)で医用生体工学の学士号、マサチューセッツ工科大学(米国)で計算システム生物学の博士号を取得。その後、ハーバードフェロー協会のジュニアフェローとなる。現在は、デューク大学(米国)准教授およびデューク微生物叢センター暫定所長。研究室では、食物と腸内微生物叢とヒトの健康の関係を調べている。研究成果は、バローズ・ウェルカム基金、サール奨学金プログラム、アーノルド・アンド・マベル・ベックマン財団、ハートウェル財団、アルフレッド・P・スローン財団、およびデーモン・ラニアン財団から、革新者賞・研究者賞を受賞している。
植物が幼児の腸になぜ重要か?
デビッド: 成人では、多様な植物を含む食物ほど微生物叢の多様性が高く、さらには良好な健康状態と関連付けられており、幼児では、多様な食物がその後のアレルギー発現リスクの低下と関連付けられています。植物性食物の主要な成分は食物繊維(複雑な炭水化物)ですが、ヒトは繊維を分解する酵素を持たず、単純な糖類やタンパク質のように吸収することができません。植物の繊維は、食べた後そのまま大腸まで達しますが、そこには極めて多くの腸内細菌が存在します。その細菌にとって繊維は重要な資源であり、繊維がないときには腸の粘液を多く食べるようになります。その結果、腸のバリア機能が損なわれ、病原体が定着するリスクが高まることがあります。しかし、こうした食物成分が幼児や小児の微生物叢の発達をどう方向付けるのか、そして特定の植物が他の植物よりも小児に有益なのかどうかについては、まだ正確にはわかっていません。微生物叢の組成はわずか数日で急変させることが可能であり、幼児の腸の健康状態を改善するための介入策は極めて迅速に奏効する可能性があります。
提案したプロジェクトの概要は?
デビッド: 小児期と幼児期は人生の中の極めて重要な時期ですが、腸内微生物叢の発達についてはわかっていることはほとんどありません。私たちのプロジェクトでは、ニカラグアのコミュニティーにおいて下痢性疾患のリスクにさらされている小児に注目します。この研究の臨床面を取り仕切る医者であり科学者でもあるシルビア・ベッカー=ドレプスは、ニカラグアのウイルス学者フィレモン・ブカルド(Filemon Bucardo)、細菌学者サミュエル・ビルチェス(Samuel Vilchez)らと共に、ニカラグアをはじめとする国々の小児の感染症リスクに影響を与える要因を、20年近くかけて調べてきました。今回私たちが提案したプロジェクトでは、幼児が成長する中で摂取する食物の多様性を評価し、それを腸内微生物叢の成熟や組成、そして幼児の全体的な健康状態と関連付けます。小児は自分が食べるものを記録できませんし、1日の中で複数の保育者に食べさせてもらうことも少なくありません。そこで、私たちの新しいメタバーコーディングツールの出番となります。このツールは、食べたものを参加者に記録させなくても、糞便試料のDNA配列を利用して、参加者の食物の摂取状況を再現します。また、そうしたデータから得られた仮説の一部を、ヒト腸モデルにおいて食物から抽出した栄養素で細菌を増殖させることで検証します。
メタバーコーディングの仕組みは?
デビッド: この技術は、アフリカのサバンナの大型草食動物の食物を研究してきた生態学者との共同研究から生まれました。食べていたものを動物に尋ねるわけにはいきませんから、生態学者たちは糞の中に残っている餌由来の残存DNAの配列を解読していました。糞に含まれるDNAの「タグ」は、植物性でも動物性でも、さまざまな食物のライブラリーと突き合わせることができ、その動物が食べたものを推測することができるのです。私たちはこの方法をヒトに応用しました。私たちは、ヒトの糞便試料に含まれる植物の葉緑体と動物のミトコンドリアのDNA塩基配列を決定します。DNA塩基配列が得られたら、それをさまざまな食物群の大規模なデータベースと照合します。現時点で、私たちのライブラリーには一般的な動植物が400種類以上登録されています。これを基に、小さい子たちが何を食べてきたのかを推測できるのです。
このプロジェクトの課題は?
デビッド: 世界には食用の植物種が何千種類もありますから、異なる文化のさまざまな食物に含まれる可能性がある全てのDNA配列を集めるために、しなければならないことがまだたくさんあります。最近行ったこのプロジェクトのパイロット研究では、糞便試料の約20%に見られたある塩基配列が、私たちのデータベースのどれとも一致しませんでした。研究代表者の1人であるテレサ・マクドナルドは、極めて重要な調査を行いました。そのDNA断片は極めて短かったため複数の植物種と一致したのですが、理論上は食べることができて、かつニカラグアに見られる植物種は、ウキクサとマランガと呼ばれる芋だけだったのです。マクドナルドは、ニカラグア国立自治大学レオン校の共同研究者に問い合わせたところ、マランガが現地で極めて一般的な幼児食の1つであることがわかりました。この芋は現地で一年を通して栽培されていて、地元では幼児の消化によいと信じられています。世界各地から加わっているメンバーが、互いの食習慣について知ることのできたこの過程は、重要で楽しいものとなりました。さらに食物は、生で食べることもあれば、煮たり、焼いたり、揚げたりすることもあるため、食物のさまざまな加工法が私たちのメタバーコーディング技術にどう影響するのかも探っています。加工の方法は、私たちがDNAから栄養の全体像を推測する能力に影響しかねないのです。
ヒトの腸のモデル化がもたらすものは?
デビッド: 私たちの人工腸モデルは、微生物叢を研究する他のグループが過去数十年にわたって行ってきた先駆的な研究に基づいています。容器の中に培地として糞便細菌を入れ、そうした細菌に個々の食物栄養素を添加して、何が起こるかを観察します。このモデルによって、摂取、消化、排便を模倣することができます。この手法にはいくつかの長所があります。まず、環境を完全に制御して、腸内生態系の特定のパラメーターを再現したり、マウスやヒト被験者では不可能な形で操作したりすることができます。また、微生物群集の動態を経時的に調べたり、異なる刺激に対する細菌の反応を数分から数時間にわたって調べたりすることもできます。
Lawrence David
このプロジェクトの実際的な応用法は?
デビッド: 低中所得国の小児のための食事ガイドラインの裏付けとなる科学的根拠を得たいと考えています。最近、ある予備的データを共同研究者に共有しましたが、ヴィルチェスは、ニカラグアの食事の特徴をそれほど詳細に示したデータは見たことがないと言っていました。そうしたデータを親たちに示し、それを疾患のリスクと結び付ければ、親たちも受け入れやすくなると思います。そのデータは自分のコミュニティーのもので、容易に理解でき、自分たちの大切なものと関連しているからです。また、特定の場所においてどのような食物が小児の食事に取り入れられているかを確認することにも価値があります。これは、地域の保健・教育プロジェクトにそのまま取り込むことができます。
将来の研究計画は?
デビッド: 小児の微生物叢の健康を増進する方法を見いだしたとしても、望ましい形で食事を変化させるには、まだ多くの課題があります。誰もがよい食事を望んでいますが、社会経済学的課題、心理と行動の変化などは、多くの場合、言うは易く行うは難しいという状況です。口にする食物が体のためになることを人々に知ってもらう方法(定期的に微生物叢をモニタリングする方法など)を編み出すことができれば、それは大きなブレークスルーになるでしょう。
Advertiser retains sole responsibility for the content of this article
審査員団紹介
審査委員の紹介審査委員は、世界各国の国際的に有名なヒト細菌叢研究者で構成されている。

ティナ・ラスク・リヒト 審査委員長

エラン・エリナフ

ポール・W・オトゥール

カレン・P・スコット

竹田 潔




