
微生物叢研究の限界を押し広げる研究をサポート
新たな生物活性物質の探索、原生生物の役割の解明、そして微生物と免疫系の相互作用のカタログ化
新奇な知見を求めて
食物過敏症において原生生物が果たす役割の解明、炎症性腸疾患(IBD)の新たな生物活性物質の発見、そして細菌叢が関連する疾患における抗体と抗原の相互作用の探索を目指す3件のプロジェクトを紹介する。
原文:In search of novel insights
2019年末、2回目となるGlobal Grants for Gut Health(GGGH)審査委員会が開かれ、応募された132のプロジェクトの中から、特に優れた提案が採択された。この分野にふさわしい用語を使うのであれば、集まった申請書は大量で多様性も実に大きいものであった。今年は、腸内細菌叢がヒトの健康に影響を及ぼす作用機序の解明に大きく貢献する、大胆で独創的な提案を探し出すことに焦点を合わせている。
我々は、GGGHによって斬新な知見が生み出させることを期待している。「新奇な(novel)」は、単に「新しい(new)」というだけの意味ではない。新奇さには、独創性、新鮮さ、独自性の含意がある。喜ばしいことに、今回の応募にはとても新奇性の高いものが多く、非常に競争力の高い応募者たちの中から3人の助成対象者が選ばれた。我々は、今年のGGGH助成対象者を祝福できることを大変うれしく思っている。
米国のピッツバーグ大学助教のラインハルト・ヒンターライトナー(Reinhard Hinterleitner)は、今回の助成金を活用して、免疫が仲介する食物過敏症における腸内の共生原生生物が果たす役割の解明を目指す。このプロジェクトは、宿主と細菌叢の相互作用に関する必要性のきわめて高い課題に取り組み、宿主と細菌叢の相互作用の十分に理解されていない側面を扱う。審査委員会は、彼の提案が独創的で時宜性があり、高度に機械論的であって、洞察に満ちた結果をもたらす可能性が高いと判断した。我々は、得られる結果について大きな期待をしている。
オーストラリアのクイーンズランド大学上級講師でIBDグループリーダーでもあるジェイコブ・ビガン(Jakob Begun)は、きわめて論理的で段階的な手法を用いて腸内細菌叢内の生物活性株を突き止めるとともに、こうした細菌株の宿主へのシグナル伝達機構に焦点を合わせている。彼は、IBDで炎症を抑制する腸内の生物活性物質を利用することを目指す。審査委員会は、その提案が、独創的で臨床的意義があり、次世代プロバイオティクス、すなわち主に生物活性の高さによって選別される、ヒト由来の生きた細菌株の探索を目指すものと判断した。
イスラエルのワイツマン科学研究所教授のエラン・セガール(Eran Segal)は、宿主と微生物の相互作用の分野で高名な研究者である。彼のプロジェクトは、大量の微生物抗原をスクリーニングするための新たな技術を開発して、疾患の予防や軽減に応用できる重要な反応を特定することを目指す。この独創的で新奇なプロジェクトは、明快な機械論的側面を持ち、膨大な既存データを基に構築されている。審査委員会は、特にその成果が科学コミュニティに公開されたときに、このプロジェクトの波及的影響が大きくなると判断した。
3件のプロジェクトは3つの大陸で実施される。これは、GGGHが世界の科学コミュニティを支援していることを反映している。3件の新奇で興味深いアプローチによって、何が生み出されるのか、そしてヒト細菌叢にまつわる多くの謎を解こうとする世界的な取り組みがどう進展するのか。我々は結果を非常に待ち遠しく思っている。
最後に、GGGHの審査委員であるエラン・エリナフ(Eran Elinav)、ポール W. オトゥール(Paul W. O’Toole)、カレン・P・スコット(Karen P. Scott)、竹田 潔、趙立平に心より御礼申しあげる。
食物アレルギーに、原生生物を勧めるべきか
免疫学者であるラインハルト・ヒンターライトナーは、Global Grant for Gut Healthの助成金で、原生生物と呼ばれる微生物が食物過敏症において保護的な役割を担っているのかを調べる。
原文:When it comes to food allergies, should we be pro-protist?

ラインハルト・ヒンターライトナー(Reinhard Hinterleitner)
ラインハルト・ヒンターライトナーは、ピッツバーグ大学免疫学科(米国)の助教である。応用科学大学(オーストリア・ウィーン)でバイオテクノロジーを学び、インスブルック医科大学(オーストリア)で博士号を取得。エルヴィン・シュレディンガー博士研究員奨励金(Erwin Schrödinger Postdoctoral Fellowship)を受け、シカゴ大学(米国)のバナ・ジャブリ(Bana Jabri)研究室に加わって、セリアック病に関連した経口耐性に対する腸内ウイルス感染の役割を研究。現在は、食物過敏症および腸の炎症との関連で腸内微生物と宿主粘膜の免疫系とのクロストークに着目している。
研究の背景は?
ヒンターライトナー: セリアック病やさまざまな食物アレルギーなど、免疫が仲介する食物過敏症の発生数が世界的に増加していることから、我々はその理由を解明する必要があります。現在のところ、唯一の現実的な治療法は、症状を引き起こす食物を食べないようにすることです。ただし食物を避けるということは、重度アレルギーを持つ人に食事制限を課し、わずかでも混入があれば命を落としかねないアレルギー反応のリスクにさらすということを意味します。食物過敏症では腸内微生物が重要な役割を果たしていることが知られています。樹状細胞は腸管から食物の抗原を絶えず取り込み、制御性T細胞を誘導することで、免疫系が食物抗原に対して「経口耐性」を確立するのを促します。これまでの研究により、腸内微生物群集のバランスの異常(「ディスバイオシス」)、特定微生物産物の欠如、ウイルス感染などの外的要因はすべて、経口耐性の喪失を引き起こす可能性があることが示されています。ディスバイオシスは、高脂肪低繊維食、抗生物質の過剰摂取、都会生活などの現代的な生活習慣によって引き起こされることがあります。腸内微生物集団を、プロバイオティクスなどの治療法によって慎重に調節する方法が見つかれば、免疫系の過剰な応答を抑えて特定の食物に対する炎症反応を防ぐことができるようになるかもしれません。
従来の細菌叢研究との違いはどこにありますか。
ヒンターライトナー: これまでの研究の多くは、腸内細菌群集と疾患との関連や相関を調べるものでした。細菌は腸内細菌叢の大部分を占めるため、アーキア、ウイルス、原生生物、菌類といったその他の重要な腸内微生物についてはあまり研究されていません。私たちのプロジェクトは、原生生物に着目します。原生生物は、かなり大きな単細胞真核微生物で、顕微鏡では泳ぎ回る姿を見ることができます。これまでの研究は、疾患を引き起こす寄生性原生生物に焦点が合わせられてきており、共生性原生生物とそれが人間の健康で果たす潜在的に有益な役割については、ほとんど分かっていません。原生生物を、食物過敏症との関連で研究した人がいないのです。私たちは、免疫応答の調節における腸内原生生物の機能と機序を、食物過敏症との関連で調べます。原生生物が誘導できると思われる興味深い免疫経路がいくつかあるため、これらを明らかにしたいと考えています。
原生生物の役割をどのように調べるのですか。
ヒンターライトナー: 私たちは、セリアック病や食物アレルギーのさまざまなマウスモデルを用いて、原生生物が免疫応答をどのように調節しているのか、また、動物モデルにおいてこうした過程が保護的な働きをしているかを調べます。腸に細菌のいない状態で飼育した無菌マウスも使います。そのマウスは実験が始まるまで、事実上、外界から隔離された状態で暮らします。このため、腸内に導入する微生物を厳密に管理することで、マウスの応答を明らかにすることができるのです。これは非常に強力なツールです。
私たちは、どの免疫細胞や免疫経路が原生生物によって調節されているのか、そしてその調節が有益なものなのかどうかを明らかにしたいと考えています。また、原生生物が免疫細胞とどのように相互作用しているのか、例えば、特定の代謝物を産生しているのかなども突き止めたいと考えています。免疫細胞が原生生物の活動に対してどのように振る舞うのかを可視化するために、さまざまな免疫細胞を染色してフローサイトメトリーを行い、免疫細胞が原生生物にどう応答し、これと相互作用するのかをモニタリングします。さらに、原生生物が、ウイルスによって引き起こされる経口耐性の喪失を防げるのかも調べます。私たちは以前、ウイルスによる経口耐性の低下がセリアック病の発症と関係していることを見いだしました。

R. Hinterleitner
知見についてどのような応用が期待されますか。
ヒンターライトナー: 今回の助成金では、食物過敏症との関連における、原生生物の保護的機能の重要性を明らかにすることができると思います。これは、今後のプロジェクトの基盤となるでしょう。動物モデルで有望であることを示すことができれば、そこから、その知見をヒトに応用できるかどうかを調べるための共同研究が促進されると期待しています。また、私たちの知見の一部を商用化したり、新たなプロバイオティクス治療に原生生物を用いたりすることも考えられます。
長期的な研究の目標は何でしょうか。
ヒンターライトナー: 私たちの研究チームは、腸内微生物が食物過敏症に影響を与えるメカニズムに注目し続けます。腸内微生物と免疫系の相互作用をよりよく理解することで、免疫応答を微調整して、副作用を生じることなく食物過敏症を予防できるようになるでしょう。理想的には、微生物を用いた製品を使って、それを実現したいと考えています。このような研究は、炎症性腸疾患(IBD)などの腸疾患や、細菌叢の影響を受ける腸以外の他の疾患の複雑さを解き明かすのにも役立つと思います。近年、多発性硬化症などの自己免疫疾患やさまざまながんと腸内微生物との関連性が明らかになってきました。異なる腸内微生物集団は免疫系を訓練するのに役立ちます。微生物のバランスが慢性的に崩れていると、免疫系は完全な状態とはならず、あらゆる種類の疾患や病態につながります。
今後この助成プログラムへの応募を考える研究者にアドバイスを。
ヒンターライトナー: 勇気を持って自分の考えに従うことが重要で、他人の指導に従う必要はありません。自分の方向性を決めて、今まで誰も調べていないものを選ぶことです。
余暇の楽しみ方は。
ヒンターライトナー: コンピュータゲームをします。自身の問題解決能力を磨けていると思います! 研究に没頭しすぎると、アイデアがすぐに枯渇してしまい、少し機械的になってしまいます。パートナーと、山でハイキングをしたり、米国内の美しい国立公園を訪れたりするのも好きです。
「薬としての微生物」と「微生物由来の薬」
生化学者であり炎症性腸疾患(IBD)の専門家でもあるジェイコブ・ビガンは、Global Grant for Gut Healthの助成金を使って、IBDの進行が微生物の力でどのように抑えられるかを探る。
原文:Bugs as drugs, and drugs from bugs

ジェイコブ・ビガン(Jakob Begun)
ジェイコブ・ビガンはケンブリッジ大学(英国)の修士課程で生化学を学び、ハーバード大学医学系大学院(米国)で医師免許および遺伝学博士号を取得。マサチューセッツ総合病院(米国)で胃腸病学および炎症性腸疾患(IBD)の高度な訓練を修了。2014年には、IBDおよび腸の健康に関する臨床・トランスレーショナル研究を行うために、オーストラリアへ渡る。現職は、メーター病院(ブリスベーン)IBDディレクター、メーター研究所IBDグループリーダー、およびクイーンズランド大学医学系大学院准教授。トランスレーショナル研究所(オーストラリア)では研究室を主宰し、自然免疫系と腸内細菌叢との相互作用、そして疾患に対する遺伝的寄与を研究している。
Global Grant for Gut Healthへの応募動機は。
ビガン: 世界的に見ると、IBDの患者数は10万人当たり約30人で、これは1型糖尿病の発症率と同等です。IBDは、慢性の消耗性疾患で、多くの場合10~20代で診断され、潰瘍性大腸炎およびクローン病という2つの主要な病態から構成されます。患者の約30%は既存の治療法が奏効しないために多くの方が手術を必要とし、障害発生率が高くなっています。今では、腸内細菌の役割や、腸内細菌が免疫系とどのように相互作用するのかについての認識が高まっています。こうした相互作用は、IBDだけでなく、関節リウマチ、ループス(狼瘡)、甲状腺疾患といった自己免疫疾患など、免疫介在性疾患全般に寄与していると考えられます。
プロジェクトの主たる目標は何でしょうか。
ビガン: IBDでは、腸内常在菌に対して不適切な免疫応答が起きています。自然免疫系、あるいは自然免疫系の腸内細菌に対する応答の仕方に不具合があると考えられます。私たちの学際的な研究チームは、細菌由来のタンパク質やその他の代謝産物に着目し、これらの分子が免疫系とどのように相互作用して免疫系を調節しているのか、免疫系がどのように応答するのかについて研究を行ってきました。これにより、腸内細菌叢が免疫系の状態をどのように整えているか、それがどのように破綻してIBDのような炎症状態をきたすのかを探ることができます。
今回のプロジェクトでは、腸内細菌が、IL-23経路という特定の炎症経路に影響を与える炎症調節性分子を産生する仕組みを調べます。私たちは、腸内細菌がこの経路をどのように標的にしているのか、そしてクローン病や潰瘍性大腸炎では本来の状態がどう乱されているのかを明らかにしたいと考えています。特に、腸内細菌がどのように機能しているのか、有益な細菌の活性を高めることで患者の免疫系のバランスを回復させて健康な状態に近づけることができるのかを調べます。
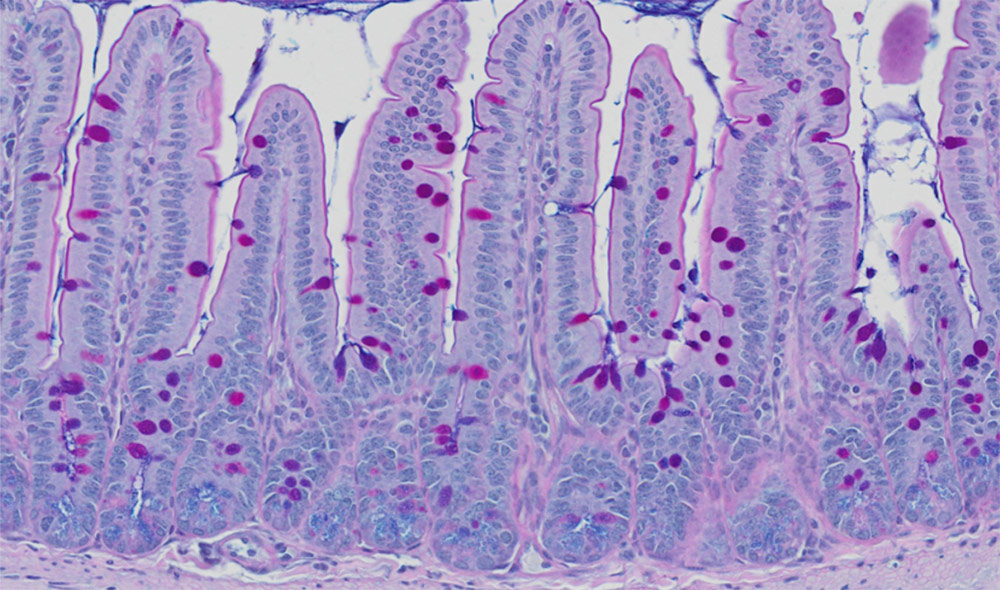
J. Begun
この経路はなぜこれまで研究されてこなかったのでしょうか。
ビガン: こうした相互作用が見過ごされてきた理由の1つは、研究が非常に困難だったためです。腸内細菌を大規模に培養して分析するのは難しいのです。ゲノミクス革命によって、腸内、そして全身に存在する細菌群集に関して、前例のない知見がもたらされています。今では、嫌気培養チャンバーや特殊な培地など、新たな細菌培養技術が登場しており、以前よりもはるかに多くの種類の細菌を培養してその機能を調べ、それらが宿主の免疫系をどのように調節しているのかを明らかにすることができるようになりました。こうした技術が、微生物研究に革命をもたらしました。
プロジェクトはどのようなステップを踏むのでしょうか。
ビガン: 私たちは、すでに健常者の糞便試料から単離した細菌のコレクションを持っています。そして、それらの中から、興味深い細菌を選択して培養を行っています。これらの単独培養系を使い、さらに細胞を用いた分析を行うことにより、細菌が免疫細胞と、特にIL-23経路とどのように相互作用するのかを調べることができます。私たちは、高度なメタボロミクスプラットフォームを使って、こうした免疫活性の基盤となっている特定の細菌由来化合物群を単離します。こうして特定された化合物のどのような側面が免疫の活性の引き金となり、活性を調節しているのかを調べます。これが新薬開発への第一歩です。
私たちは、動物モデルを用いて、こうした細菌由来の化合物が免疫応答を調節していることを検証します。また、これらの細菌由来化合物が、IBDコホートから得たヒト由来の試料において免疫シグナル伝達に影響を与えるのかどうかも調べる予定です。このプロジェクトの期間内に、私たちの細菌ライブラリーから、新たな治療法の開発につながる特定の候補物質を見いだしたいと考えています。
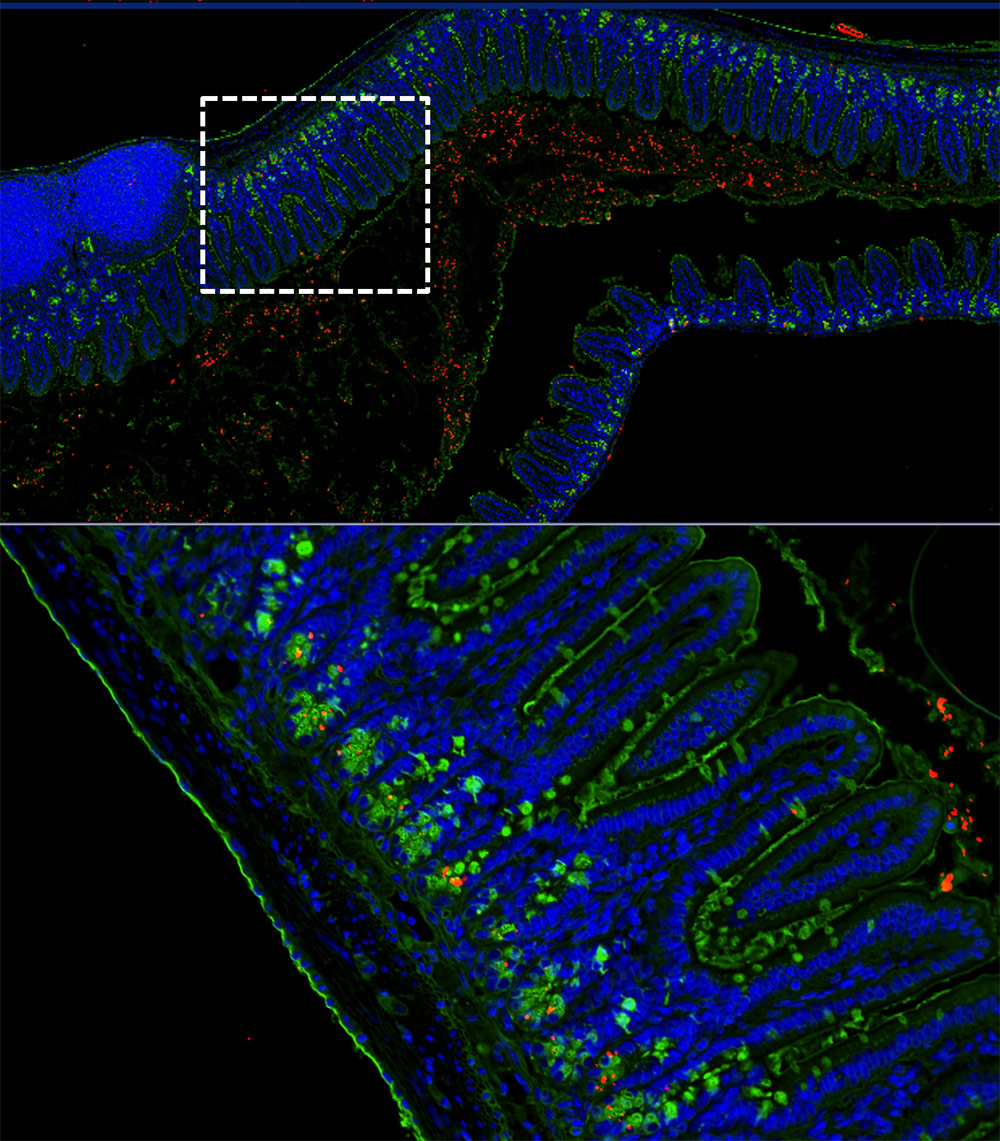
J. Begun
プロジェクトの実際的な応用法にはどのようなものがありますか。
ビガン: 2つの包括的な原理があります。1つは「薬としての微生物(bugs as drugs)」というアプローチで、発見した細菌を取り出し、それを優れたプロバイオティクスとして開発するものです。このアプローチでは、治療法を個別化することができます。例えば、炎症活性を抑えることのできる20の細菌株からなるコレクションを、患者の血液試料に対して試験することができます。実際の治療法は、その患者の免疫系に対する効果が高い6株の細菌で構成されることになるかもしれません。まもなく、プロバイオティクス療法に対する意思決定に基づいたアプローチをとれるようになると思います。
第2の原理は「微生物由来の薬(drugs from bugs)」です。このアプローチでは、特定した細菌化合物を使って、IL-23に対して高い親和性と活性を持つ薬剤を設計します。どちらのアプローチも、IBD以外の疾患にも有用な可能性があり、免疫介在性の他の健康関連状態に対する有用性が証明されるかもしれません。
趣味は何ですか。
ビガン: セーリングが好きで、両親とよく一緒に出かけています。スキーも大好きです。学会はスキー場の近くで開催されることも多く、ゲレンデで仲間と一緒に楽しみます。サイクリングも大好きです。また、子どもたちとさまざまな活動に参加しています。
この助成プログラムへ応募する研究者にアドバイスを。
ビガン: 短期間に実現可能でありながら、この研究領域に大きなインパクトを与える可能性があるプロジェクトを提案することが重要だと思います。細菌叢研究全体に大きな注目が集まっています。特に、人間という「ホロビオント(宿主およびそれと共生関係にある生物の集合体)」についての知識が深まれば深まるほど、ホロビオントという1つの生命体が、私たちが生物として機能する多くをカバーしているためです。結局のところ、私たちのDNAは、私たちがヒトである以上に微生物的であることが分かったのです。
細菌叢と免疫系の相互作用を調べるための新たなスクリーニング法
計算生物学者のエラン・セガールは、Global Grant for Gut Healthの助成金を使って、細菌叢と免疫系がどのように相互作用するのか、そしてそれがどのように不調をきたすのかを調べる。
原文:Novel screening approach to study microbiome-immune interactions

エラン・セガール(Eran Segal)
セガールは、ワイツマン科学研究所計算科学・応用数学科(イスラエル)の教授で、計算システム生物学分野の計算生物学者と実験科学者からなる学際的チームの研究室を主宰している。彼らのグループは、機械学習、計算生物学、不均一なハイスループットゲノムデータの解析に関する経験が豊富である。研究テーマは、細菌叢、栄養学、遺伝学、そしてそれらが健康と疾患に与える影響であり、その目標は、ヒトコホートから得られたビッグデータに基づいた個別化医療を開発することである。
細菌叢研究に興味を持つようになった時期は。
セガール: 私はマラソンを走るのが大好きで、そのため、栄養学に強い関心を持つようになり、細菌叢がフィットネス食にどのように応答するのかに強い興味がわきました。私はもともと遺伝子調節という別の計算生物学分野からこの道に入ったのですが、栄養学に対する関心が高まるにつれ、細菌叢学が急速に発展している新しい研究分野であることを知り、それに取り組みたいと熱望するようになったのです。私たちは、独自の新しい免疫学的手法を用いて個別化栄養プロジェクトに取り組んできており、そこから、新たな研究にすぐに使える我々のコホート由来の試料コレクションや、新たな研究の技術的基盤が得られました。
プロジェクトのテーマは。
セガール: 健康には免疫系と細菌叢の両方が重要であることはすでに知られています。免疫系と細菌叢が相互作用しており、ヒトの体は腸内細菌に対する抗体を毎日約2g産生していることも分かっています。体を健康な状態に保つには、細菌叢と免疫応答との絶妙なバランスが必要です。しかし、免疫系と細菌叢の相互作用がどの程度広範なものかについては、測定や分析を大規模に行うことができないため、ほとんど分かっていませんでした。通常、1つの研究プロジェクトでは、免疫系の特定の1つの遺伝子について、特定の1種の細菌との相互作用を調べます。私たちのプロジェクトは、初めて、健康な人と自己免疫疾患と自己炎症性疾患の患者の両方で、免疫系と細菌叢の相互作用の包括的なマッピングを行います。私たちは、腸内の抗原に対するどういった免疫応答が、疾患を引き起こしたり悪化させたりする可能性があるのかを突き止めたいと考えています。私たちは、機械学習、ファージディスプレイ技術、ロボットオートメーションを組み合わせて、何十万件もの分子相互作用を体系的に識別できる先駆的なハイスループット法を考案しました。これによって、免疫系と細菌叢が、健康な状態と疾患状態においてどのように相互作用しているかについての詳細なプロファイルがもたらされるはずです。
新しいスクリーニング法の仕組みは。
セガール: 我々は、炎症性腸疾患(IBD)患者250例、多発性硬化症(MS)患者250例、そして500人の対照健常者から採取した計1000点の細菌叢試料から、特に量が多い細菌や興味深い細菌を選別します。そして、その細菌の中から、分泌タンパク質や膜タンパク質など、免疫系によって認識されやすい分子領域を持つ特定の抗原を選択します。そうした抗原のデザインを何十万点もコンピューターに登録して、合成へと進めます。私たちはこうして合成した抗原を用いて、ファージライブラリーを作製します。ライブラリーでは、各ファージが特定の抗原を提示していて、その抗原の生成に用いられたDNAを保持しています。次に、人間の血液試料を採取します。それぞれの血液試料にはその人に固有の抗体群が含まれており、この試料をファージライブラリーとともにインキュベートします。ある特定の抗原を認識する抗体があれば、その抗体と抗原が結合します。結合した抗原–抗体複合体はすべて回収して、ファージDNAの次世代シーケンシングを行うことができます。これにより、元のライブラリーと比較してどのDNA要素が濃縮されているかが分かるわけです。濃縮結果は、その特定の抗原がその人の抗体によってどれだけ選択されたのかを示しています。私たちは、苦心してシステムを慎重に較正し、SN比(信号対雑音比)を高めました。この技術の信頼性はとても高いものです。1回の実験で、任意の血液試料に対して最大100万個の抗原を調べることができるうえ、最大100点の試料を同時に分析することができます。
nobeastsofierce/Shutterstock
結果から得られる知見は。
セガール: それぞれの人について、免疫系がどの微生物抗原を認識しているかを明らかにすることができます。さらにこの分析結果は、その個人の他の健康データと関連付けることができます。これにより、IBDやMSと微生物活性との直接的な関係、そしてうまくいけば、こうした疾患の潜在的バイオマーカーを突き止めることができるのです。
私たちは幅広い問題に答えるように努めています。例えば、あなたの現在の細菌叢構成と、免疫系がこれらの細菌群から認識しているものとの間に関係があるのでしょうか。おそらく、免疫系は、特定の細菌を能動的に排除しています。免疫系は、細菌を危険なもの、あるいは不耐症の原因として認識していたり、どの細菌が安全で、どの細菌が共生細菌叢に属しているかをチェックしたりしているのです。
具体的な例を挙げましょう。リーキーガット(腸管壁浸漏)です。この病態は、肥満や糖尿病などの疾患に関与しています。この状態になると、細菌が腸内から漏れ出し、体内の別の部位に移ります。運がよければ、免疫系がその細菌を阻止します。しかし、免疫系による阻止が完全でない場合、腸内から漏れ出した細菌が炎症を引き起こします。我々の技術は、腸管壁浸漏の人、あるいは過去に症状のあった人の免疫系に残された痕跡を発見できると思います。我々の技術はまた、シグナルの程度も分かるので、その人の腸管壁浸漏の重篤度に関する情報も得られるはずです。
知見について長期的にはどのような応用が期待されますか。
セガール: 私たちの研究は、第一に、現在の科学的知識に貢献して、免疫系と細菌叢との相互作用に関する基礎的理解を深めます。第二に、さまざまな疾患の診断や予後判定、治療介入効果の評価を行うための有用な検査法の開発に役立つバイオマーカーを発見します。私たちが発見する免疫系の痕跡は、新しい治療法の開発において重要である可能性があります。究極的には、この技術基盤によって、個々人が許容できない抗原を簡便かつ効率的な検査で明らかにすることで、医療の個別化に役立つ可能性もあります。私たちが開発した技術の対象はとても幅広く、あらゆる抗原に対する免疫応答を調べることができるのです。
Advertiser retains sole responsibility for the content of this article
審査員団紹介
審査委員は、世界各国の国際的に有名なヒト細菌叢研究者で構成されている。

ティナ・ラスク・リヒト 審査委員長

エラン・エリナフ

ポール・W・オトゥール

カレン・P・スコット

竹田 潔




